Une étude menée sur des souris par des scientifiques du Eli et Edythe Broad Center of Regenerative Medicine and Stem Cell Research de l’UCLA révèle que les cellules du muscle cardiaque jouent un rôle central dans la détermination de la façon dont le cœur guérit après une crise cardiaque. Les résultats remettent en question un paradigme de longue date sur la réparation cardiaque et identifient une protéine qui pourrait servir de cible à des médicaments pour traiter ou prévenir l’insuffisance cardiaque.

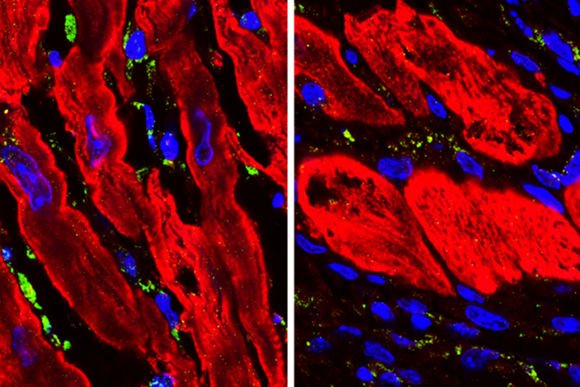
Images microscopiques montrant du tissu cardiaque chez la souris (avec des cellules musculaires cardiaques en rouge) après une crise cardiaque. Les tissus non traités (à gauche) présentent plus de dommages à l’ADN (en vert) que les tissus qui ont été traités avec un médicament expérimental (à droite). Crédit : Centre de recherche sur les cellules souches larges de l’UCLA
Fond
La crise cardiaque est la principale cause d’insuffisance cardiaque, qui tue plus de 600 000 personnes aux États-Unis chaque année. Une réponse de réparation optimale est essentielle pour minimiser la quantité de cicatrices après une crise cardiaque car, une fois formé, le tissu cicatriciel cardiaque reste à vie et réduit la capacité du cœur à pomper le sang. Cela ajoute une tension au muscle cardiaque restant qui, avec le temps, peut conduire au développement d’une insuffisance cardiaque.
Le tissu musculaire cardiaque est constitué de cellules musculaires cardiaques, qui sont responsables de la capacité du cœur à pomper le sang. Étant donné que ces cellules ont une capacité d’auto-réplication très limitée, elles sont incapables de générer suffisamment de cellules musculaires cardiaques pour remplacer le tissu endommagé lors d’une crise cardiaque. Au lieu de cela, le cœur produit du tissu cicatriciel pour préserver son intégrité structurelle. On pensait que les cellules du muscle cardiaque jouaient un rôle minime dans la cicatrisation et le processus de réparation du cœur.
Méthode
Les chercheurs ont étudié les tissus du cœur de souris en bonne santé et le cœur de souris qui se trouvaient dans les trois premières semaines de récupération après une crise cardiaque. Les scientifiques ont découvert que les échantillons de tissu cardiaque des souris post-crise cardiaque présentaient des niveaux accrus d’une protéine appelée ENPP1.
Ensuite, ils ont découvert que l’ENPP1 transforme l’ATP, une molécule libérée par les cellules du muscle cardiaque mourantes, en une autre molécule appelée AMP. Les cellules musculaires cardiaques survivantes perçoivent la présence d’AMP comme un signal indiquant que le cœur est attaqué, ce qui les incite à libérer des molécules spécifiques qui provoquent la mort des cellules non musculaires qui les entourent. Les chercheurs ont découvert que le blocage de la production d’ENPP1 améliorait la réparation cardiaque et réduisait la formation de tissu cicatriciel, ce qui à son tour conduisait à une amélioration de la fonction cardiaque.
Impacter
La moitié des personnes atteintes d’insuffisance cardiaque meurent dans les cinq ans suivant leur diagnostic, et il n’existe actuellement aucun médicament qui améliore le processus de réparation du cœur après une crise cardiaque. La nouvelle étude suggère comment le processus de réparation pourrait être modulé pour améliorer les résultats et identifie des cibles moléculaires spécifiques pour les nouveaux médicaments. Les chercheurs étudient actuellement un médicament candidat qui inhibe efficacement ENPP1 chez la souris et dans les cellules musculaires cardiaques dérivées de cellules souches humaines.
Le financement
Le travail a été financé par les National Institutes of Health, le ministère de la Défense, le University of California Center for Accelerated Innovation et le University of California Drug Discovery Consortium, et par une subvention à l’innovateur de la Fondation Rose Hills du Broad Stem Cell Research Center de l’UCLA.
Divulgations
Le candidat thérapeutique décrit dans cette étude est couvert par une demande de brevet déposée par le UCLA Technology Development Group au nom des Regents de l’Université de Californie, avec Arjun Deb répertorié comme inventeur. La stratégie de traitement n’a été utilisée que dans les tests précliniques ; il n’a pas été testé chez l’homme ni approuvé par la Food and Drug Administration des États-Unis comme étant sûr et efficace pour une utilisation chez l’homme.
Référence:
Shen Li, et al. “Le cardiomyocyte perturbe la biosynthèse de la pyrimidine dans les non-myocytes pour réguler la réparation cardiaque“. Le Journal d’Investigation Clinique (2021).
La source: UCLA, par Tiare Dunlap.