Le SRAS-CoV-2 dépend de manière critique d’un mécanisme spécial pour la production de ses protéines. Une équipe de collaboration dirigée par un groupe de recherche de l’ETH Zurich a obtenu des informations moléculaires sur ce processus et a démontré qu’il pouvait être inhibé par des composés chimiques, réduisant ainsi considérablement la réplication virale dans les cellules infectées.

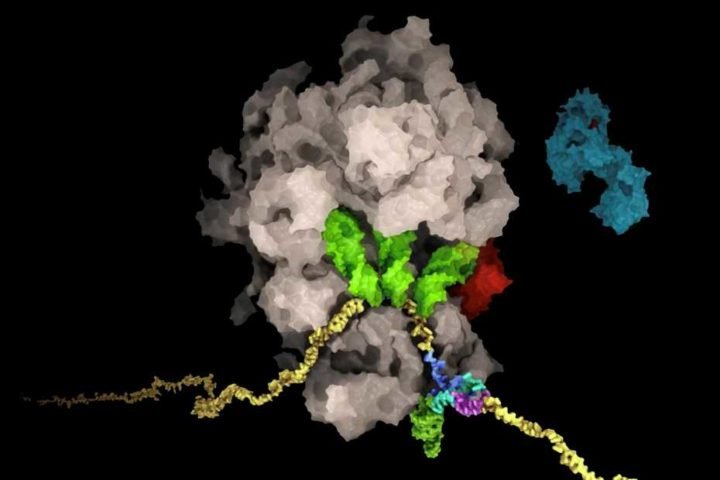
L’ARN (jaune) du virus SRAS-CoV-2 forme une structure pseudoknot (multicolore, en bas à droite) qui conduit à un décalage du cadre de lecture du ribosome (marron). De cette manière, l’ARN viral contrôle les niveaux de production des protéines virales. Pour plus d’informations, regardez la vidéo ci-dessus. Crédit d’image: Said Sannuga, Cellscape.co.uk / ETH Zurich, The Ban Lab
Les virus ont besoin des ressources d’une cellule infectée pour se répliquer, puis infecter d’autres cellules et se transférer à d’autres individus. Une étape essentielle du cycle de vie viral est la production de nouvelles protéines virales basées sur les instructions du génome de l’ARN viral. Sur la base de ces plans de construction, la propre machine de synthèse des protéines de la cellule, appelée ribosome, produit les protéines virales.
En l’absence d’infection virale, le ribosome se déplace le long de l’ARN selon des étapes strictement définies, lisant trois lettres d’ARN à la fois. Ce code à trois lettres définit l’acide aminé correspondant qui est attaché à la protéine en croissance. Il n’arrive presque jamais que le ribosome glisse une ou deux lettres d’ARN vers l’avant ou vers l’arrière au lieu de suivre les étapes régulières de trois lettres. Lorsqu’un tel glissement du ribosome se produit, on parle de «décalage de cadre» et cela conduit à une lecture incorrecte du code génétique.
Le décalage du cadre ne se produit presque jamais dans nos cellules. Cela conduirait à des protéines cellulaires dysfonctionnelles; cependant, certains virus, tels que les coronavirus et le VIH, dépendent d’un événement de changement de cadre pour réguler les niveaux de protéines virales. Par exemple, le SRAS-CoV-2 – le virus qui cause le COVID-19 – dépend de manière critique du décalage de cadre favorisé par un repli inhabituel et complexe de l’ARN viral.
Par conséquent, étant donné que le décalage de cadre est essentiel pour le virus mais qu’il ne se produit presque jamais dans notre organisme, tout composé qui inhibe le décalage de cadre en ciblant ce repli d’ARN pourrait potentiellement être utile en tant que médicament pour lutter contre l’infection. Cependant, jusqu’à présent, il n’y a aucune information sur la façon dont l’ARN viral interagit avec le ribosome pour favoriser le décalage du cadre, ce qui serait important pour le développement de médicaments.
Image détaillée d’un processus essentiel pour la réplication du coronavirus
Une équipe de chercheurs de l’ETH Zurich et des universités de Berne, Lausanne et Cork (en Irlande) a pour la première fois réussi à révéler les interactions entre le génome viral et le ribosome lors du décalage de cadre. Leurs résultats viennent d’être publiés dans la revue La science.
À l’aide d’expériences biochimiques sophistiquées, les chercheurs ont réussi à capturer le ribosome sur le site de décalage de cadre du génome ARN du SRAS-CoV-2. Ils pourraient ensuite étudier ce complexe moléculaire à l’aide de la cryo-microscopie électronique.
Les résultats ont fourni une description moléculaire du processus avec des détails sans précédent et ont révélé un certain nombre de nouvelles caractéristiques inattendues. L’événement de décalage de cadre amène la machine à ribosomes généralement dynamique à adopter une conformation tendue, ce qui a contribué à fournir l’une des images les plus nettes et les plus précises d’un ribosome de mammifère, visualisé dans le processus de décalage de cadre lors de la lecture des informations du génome viral. Les chercheurs ont ensuite suivi leurs découvertes structurelles avec in vitro et dans vivo expériences, y compris l’exploration de la manière dont ce processus peut être ciblé avec des composés chimiques Nenad Ban, professeur de biologie moléculaire à l’ETH Zurich et co-auteur de l’étude, souligne que «les résultats présentés ici sur le SRAS-CoV-2 seront également utiles pour comprendre les mécanismes de changement de cadre dans d’autres virus à ARN».
Cible possible pour le développement de médicaments antiviraux
La dépendance du SRAS-CoV-2 à cet événement de décalage de cadre ribosomal pourrait être utilisée pour développer des médicaments antiviraux. Des études antérieures ont rapporté que plusieurs composés sont capables d’inhiber le décalage de cadre dans les coronavirus, cependant, cette étude fournit maintenant des informations sur les effets de ces composés sur les niveaux de SRAS-CoV-2 dans les cellules infectées.
Dans leurs expériences, les deux composés ont réduit la réplication virale de trois à quatre ordres de grandeur et n’étaient pas toxiques pour les cellules traitées. Cependant, l’un des deux a réduit la réplication virale en inhibant le décalage de cadre ribosomal, tandis que l’autre pourrait agir par un mécanisme différent.
Bien que ces composés ne soient actuellement pas assez puissants pour être utilisés comme médicaments thérapeutiques, cette étude démontre que l’inhibition du décalage de cadre ribosomal a un effet profond sur la réplication virale, ce qui ouvre la voie au développement de meilleurs composés. Étant donné que tous les coronavirus dépendent de ce mécanisme de décalage de cadre conservé, un médicament qui cible ce processus peut même être utile pour traiter les infections par des coronavirus plus éloignés. «Nos travaux futurs se concentreront sur la compréhension des mécanismes de défense cellulaire qui suppriment le décalage du cadre viral, car cela pourrait être utile pour le développement de petits composés ayant une activité similaire», déclare Ban.
La source: ETH Zurich